Электрохимическая защита трубопроводов от коррозии — электронный каталог продукции,разработка мобильных приложений,АОС,автоматизированные обучающие системы,семинары по нефтегазовой тематике,разработка СТУ,СТУ
Электрохимическая защита от коррозии состоит из катодной и дренажной защиты. Катодная защита трубопроводов осуществляется двумя основными методами: применением металлических анодов-протекторов (гальванический протекторный метод) и применением внешних источников постоянного тока, минус которых соединяется с трубой, а плюс — с анодным заземлением (электрический метод).Рис. 1. Принцип работы катодной защиты
Гальваническая протекторная защита от коррозии
Наиболее очевидным способом осуществления электрохимической защиты металлического сооружения, имеющего непосредственный контакт с электролитической средой, является метод гальванической защиты, в основу которого положен тот факт, что различные металлы в электролите имеют различные электродные потенциалы.
В качестве основных материалов для изготовления протекторов используются магний, алюминий и цинк. Из сопоставления свойств магния, алюминия и цинка видно, что из рассматриваемых элементов магний обладает наибольшей электродвижущей силой. В то же время одной из наиболее важных практических характеристик протекторов является коэффициент полезного действия, показывающий долю массы протектора, использованной на получение полезной электрической энергии в цепи. К.П.Д. протекторов, изготовленных из магния и магниевых сплавов, редко превышают 50 % в, в отличие от протекторов на основе Zn и Al с К.П.Д. 90 % и более.
Рис. 2. Примеры магниевых протекторов
Обычно протекторные установки применяются для катодной защиты трубопроводов, не имеющих электрических контактов со смежными протяженными коммуникациями, отдельных участков трубопроводов, а также резервуаров, стальных защитных кожухов (патронов), подземных резервуаров и емкостей, стальных опор и свай, и других сосредоточенных объектов.
В то же время протекторные установки очень чувствительны к ошибкам в их размещении и комплектации. Неправильный выбор или размещение протекторных установок приводит к резкому снижению их эффективности.
Катодная защита от коррозии
Наиболее распространенный метод электрохимической защиты от коррозии подземных металлических сооружений — это катодная защита, осуществляемая путем катодной поляризации защищаемой металлической поверхности. На практике это реализуется путем подключения защищаемого трубопровода к отрицательному полюсу внешнего источника постоянного тока, называемого станцией катодной защиты. Положительный полюс источника соединяют кабелем с внешним дополнительным электродом, сделанным из металла, графита или проводящей резины. Этот внешний электрод размещается в той же коррозионной среде, что и защищаемый объект, в случае подземных промысловых трубопроводов, в почве. Таким образом, образуется замкнутая электрическая цепь: дополнительный внешний электрод — почвенный электролит — трубопровод — катодный кабель — источник постоянного тока — анодный кабель.
Таким образом, система катодной защиты состоит из защищаемого сооружения, источника постоянного тока (станции катодной защиты), анодного заземления, соединительных анодной и катодной линий, окружающей их электропроводной среды (почвы), а также элементов системы мониторинга — контрольно-измерительных пунктов.
Дренажная защита от коррозии
Дренажная защита трубопроводов от коррозии блуждающими токами осуществляется путем направленного отвода этих токов к источнику или в землю. Установка дренажной защиты может быть нескольких видов: земляной, прямой, поляризованный и усиленный дренажи.
Рис. 3. Станция дренажной защиты
Земляной дренаж осуществляется заземлением трубопроводов дополнительными электродами в местах их анодных зон, прямой дренаж — созданием электрической перемычки между трубопроводом и отрицательным полюсом источника блуждающих токов, например рельсовой сетью электрифицированной железной дороги. Поляризованный дренаж в отличие от прямого обладает только односторонней проводимостью, поэтому при появлении положительного потенциала на рельсах дренаж автоматически отключается. В усиленном дренаже дополнительно в цепь включается преобразователь тока, позволяющий увеличивать дренажный ток.
P.S. Обзор технических решений по ЭХЗ других металлических конструкций и сооружений можно прочитать здесь.
Хотите узнать больше о коррозии металлических конструкций и методах противокоррозионной защиты?
Скачайте наше специализированное учебно-справочное приложение «Защита от коррозии»
Принцип действия электрозащиты | corrosio.
 ru
ruКак известно из предыдущей статьи «Защита от коррозии» — потенциал защищаемого металла может быть изменен, если использовать внешний источник напряжения. Это составляет основу электрохимического метода защиты от коррозии (электрозащита).
Для того, чтобы наглядно увидеть действие электрозащиты целесообразно привести следующий эксперимент.
В стакан или небольшую стеклянную банку с раствором электролита поместите две небольшие стальные пластины. К пластинам подсоедините провода и соберите схему (см. рис. 1). Переменный резистор должен иметь сопротивление порядка 500-1000 Ом. В качестве источника напряжения 12 В можно использовать аккумуляторную батарею, или набор батареек. После того как все соединения выполнены, можно приступать к эксперименту. Левый по схеме электрод будет катодом, правый — анодом.
С помощью переменного резистора R можно изменять разность потенциалов между электродами, изменяя тем самым скорость коррозии защищаемого металла (катода). Разность потенциалов определяется с помощью вольтметра V.
Разность потенциалов определяется с помощью вольтметра V.
При нахождении ползунка резистора в точке А разность потенциалов между электродами равна нулю, и оба металла корродируют с одинаковой скоростью. Процесс коррозии характеризуется довольно низкой скоростью и, вообще говоря, необходимо несколько дней, чтобы увидеть явные признаки ржавчины на металле.
Если передвигать ползунок резистора от точки А к точке Б, то разность потенциалов будет увеличиваться. При положительных показаниях вольтметра образуется защитный потенциал, который полностью остановит процесс коррозии катода. При этом можно будет наглядно наблюдать выделение водорода на катоде и процесс образования ржавчины на аноде. В данном случае анод, имеющий положительный потенциал, будет притягивать к себе гидроксильные группы (ОН) из раствора электролита и окислиться, а избыточные электроны под действием внешнего источника напряжения будут переходить на катод и восстанавливать его. Для увеличения скорости реакции достаточно растворить в банке с водой половину чайной ложки поваренной соли.
Теоретически, для полного прекращения коррозии, необходимо обеспечить защитный потенциал, равный стандартному электродному потенциалу защищаемого металла, который для железа равен 0,44 В. В действительности же различные включения в железо вызывают продолжение процесса коррозии. Для предотвращения этого явления необходимо дополнительно увеличить разность потенциалов между анодом и катодом.
Обращаясь вновь к экспериментальной установке, можно видеть, что с увеличением разности потенциалов резко возрастает интенсивность выделения водорода на катоде. Происходит это потому, что одновременно с увеличением разности потенциалов возрастает и ток между электродами, который и приводит к наблюдаемому эффекту.
Многочисленные исследования показали, что сила тока между электродами зависит от состояния защищаемой поверхности, в том числе от наличия защитного лакокрасочного покрытия и может изменяться от 0,05 мА (при хорошем состояние металла) до 10 мА (при нарушенном лакокрасочного покрытии) на каждый квадратный метр защищаемой поверхности.
технология, виды и средства защиты труб и трубопроводов от коррозии
Трубопроводные магистрали сегодня являются наиболее распространенным средством для осуществления доставки носителей энергии. К сожалению, у них есть существенный недостаток – они подвержены образованию ржавчины. Чтобы избежать появления коррозии на магистральных трубопроводах, выполняют катодную защиту. В чем же заключается ее принцип действия?
В наши дни существует много способов защиты водопроводов от коррозии. Суть их проста: металл, из которого изготовлены трубы, вступает в реакцию с определенными растворами и веществами. Результатом процесса становится образование небольшой защитной пенки.
Специалистами выделяются следующие методы защиты трубопроводов от коррозии:
Электрохимическая защита
Достаточно результативный способ защиты металлоконструкций от электрохимической коррозии.
Восстановление покрытия трубопровода, расположенного под землей, или днища морского судна – процесс достаточно трудоемкий и дорогой, а в некоторых случаях и невозможный. Благодаря электрохимической защите изделие будет надежно защищено от коррозии: покрытия подземных трубопроводов, днищ судов, всевозможных резервуаров не будут разрушаться.
- Используется метод в ситуациях, когда потенциал свободной коррозии пребывает в области усиленного распада основного металла или перепассивации. То есть, когда металлоконструкция интенсивно разрушается.
-
При электрохимической защите к изделию из металла подключают постоянный электрический ток. Благодаря ему на поверхности металлической конструкции образуется катодная поляризация электродов микрогальванических пар и анодные области становятся катодными.

- Электрохимическая защита может быть анодной или катодной: это будет зависеть от того, в какую сторону сдвинется потенциал металла (в положительную или в отрицательную).
Катодная защита
Метод, достаточно часто используемый для защиты металлоконструкций от коррозии. Применяется в тех случаях, когда металл не имеет склонности к пассивации. Суть метода проста: к изделию подается внешний электроток от отрицательного полюса, который обеспечивает поляризацию катодных участков коррозионных составляющих и поднимает значение потенциала до анодных. После прикрепления положительного полюса источника тока к аноду коррозия защищаемого изделия становится почти нулевой.
Анод требует периодической замены, так как со временем происходит его разрушение.
-
Способы катодной защиты: поляризация от внешнего источника электротока, торможение развития катодного процесса, связь с металлом, имеющим более электроотрицательный потенциал свободной коррозии в определенной среде (протекторная защита).

- С помощью поляризации от внешнего источника электротока защищают конструкции, находящиеся в почве и в воде, цинк, олово, алюминий и его сплавы, титан, медь и ее сплавы, свинец, высокохромистые, углеродистые, низколегированные и высоколегированные стали.
- Роль внешнего источника электротока выполняют станции катодной защиты. Их главные составляющие — выпрямитель, токоподвод к защищаемому объекту, анодные заземлители, электрод сравнения и анодный кабель.
- Катодная защита может быть использована в качестве самостоятельного или дополнительного способа коррозионной защиты.
Основной показатель результативности метода – защитный потенциал. Защитным называют тот потенциал, при котором быстрота коррозионного процесса металлического изделия становится минимальной.
Однако катодная защита обладает определенными недостатками. Один из них – опасность перезащиты. Такой эффект может наблюдаться в случае большого смещения потенциала защищаемого изделия в отрицательную сторону. Вследствие этого разрушаются защитные оболочки, начинается водородное охрупчивание металла, коррозионное растрескивание.
Вследствие этого разрушаются защитные оболочки, начинается водородное охрупчивание металла, коррозионное растрескивание.
Протекторная защита
Вид катодной защиты, в процессе которого к защищаемому объекту подсоединяют металл с более высоким электроотрицательным потенциалом. При этом разрушается не металлоконструкция, а протектор. Через определенный промежуток времени протектор корродирует и его потребуется заменить на новый.
- Эффект от протекторной защиты будет заметен только в том случае, если переходное сопротивление между протектором и окружающей средой незначительно.
- У каждого протектора есть свой радиус защитного действия – предельно возможное расстояние, на которое можно удалить протектор без утраты защитного эффекта. Протекторную защиту применяют, когда ток к объекту подвести трудно, дорого или просто невозможно.
-
С помощью протекторов защищают объекты, находящиеся в нейтральных средах (море, реке, воздухе, почве и т.
 д.).
д.). - Материалом для изготовления протекторов служит магний, цинк, железо, алюминий. Металлы в чистом виде не смогут стать эффективной защитой для конструкций, поэтому, изготавливая протекторы, их дополнительно легируют.
Для изготовления железных протекторов используют углеродистые стали или чистое железо.
Анодная защита
Используется для титановых конструкций, объектов из низколегированных нержавеющих, углеродистых сталей, железистых высоколегированных сплавов, разнородных пассивирующихся металлов. Метод применяют в хорошо электропроводной коррозионной среде.
При анодной защите происходит сдвиг потенциала защищаемого металла в более положительную сторону. Смещение будет длиться до тех пор, пока не достигнется инертное устойчивое состояние системы. К преимуществам анодной электрохимической защиты можно отнести не только существенное торможение скорости коррозии, но и то, что продукты коррозии не оказываются в производимом продукте и среде.
- Существует несколько способов реализации анодной защиты: можно сдвинуть потенциал в положительную сторону с помощью источника внешнего электротока или ввести в коррозионную среду окислители, которые способны повысить эффективность катодного процесса на металлической поверхности.
- Анодная защита с применением окислителей по защитному механизму имеет много общего с анодной поляризацией.
- При использовании пассивирующих ингибиторов с окисляющими характеристиками (бихроматов, нитратов и т.д.), защищаемая металлическая поверхность под воздействием возникшего тока становится пассивной. Однако эти вещества способны сильно загрязнять технологическую среду.
- Если ввести в сплав добавки, реакция восстановления деполяризаторов, которая происходит на катоде, пройдет не с таким большим перенапряжением, как на защищаемом металле.
-
При прохождении электротока через защищаемую конструкцию потенциал сдвигается в положительную сторону.

- В состав установки для анодной электрохимической защиты входит источник внешнего электротока, электрод сравнения, катод и защищаемая конструкция.
Для эффективности метода в той или иной среде используют легкопассивируемые металлы и сплавы. Кроме этого требуется высокое качество выполнения соединительных элементов и постоянное нахождение электрода сравнения и катода в растворе.
Подход к проектированию схемы расположения катодов должен быть индивидуальным для каждого случая.
Электрохимическую анодную защиту нержавеющих сталей используют для хранилищ серной кислоты, аммиачных растворов, минеральных удобрений, различных сборников, цистерн, мерников.
Анодную защиту используют, чтобы предотвратить коррозию ванн химического никелирования и теплообменных установок в изготовлении искусственного волокна и серной кислоты.
Электродренажная защита
Это способ защиты трубопроводов от разрушения с помощью блуждающих токов. Метод предусматривает их дренаж (отвод) с защищаемой конструкции на источник блуждающих токов или специальное заземление.
Метод предусматривает их дренаж (отвод) с защищаемой конструкции на источник блуждающих токов или специальное заземление.
- Дренаж бывает прямым, поляризованным и усиленным. Прямой электрический дренаж — это дренажное устройство, имеющее двустороннюю проводимость. При величине тока, превышающей допустимую величину, выйдет из строя плавкий предохранитель. Электрический ток пойдет по обмотке реле, оно включится, после чего произойдет включение звука или света.
- Прямой электрический дренаж используют для тех трубопроводов, чей потенциал всегда выше потенциала рельсовой сети, служащей для отвода блуждающих токов. Иначе отвод станет каналом для натекания блуждающих токов на трубопровод.
-
Поляризованный электрический дренаж является дренажным устройством, имеющим одностороннюю проходимость. Отличие поляризованного дренажа от прямого заключается в присутствии у первого элемента односторонней проводимости ВЭ.
 В случае поляризованного дренажа ток течет только в одном направлении — от трубопровода к рельсу. Это не позволяет блуждающим токам натекать на трубопровод по дренажному проводу.
В случае поляризованного дренажа ток течет только в одном направлении — от трубопровода к рельсу. Это не позволяет блуждающим токам натекать на трубопровод по дренажному проводу. - Усиленный дренаж используется тогда, когда требуется не только отвести блуждающие токи с трубопровода, но и создать на нем определенную величину защитного потенциала. Усиленный дренаж – это обычная катодная станция. Ее отрицательный полюс подсоединяют к защищаемой конструкции, а положительный — к рельсам электрифицированного транспорта, а не к анодному заземлению.
- Как только трубопровод введут в эксплуатацию, регулируют работу системы его защиты от коррозии. Если возникает необходимость, осуществляют подключение станций катодной и дренажной защиты и протекторных установок.
Использование какой-либо из технологий защиты промысловых, стальных и прочих видов трубопроводов от коррозии – обязательная составляющая их эксплуатации. Все методы антикоррозийной защиты требуется реализовывать в строгом соответствии с ГОСТом.
Электрохимическая защита кузова автомобиля от коррозии
Одним из наиболее распространенных и в то же время губительных факторов, воздействующих на автомобиль в процессе эксплуатации, выступает коррозия. Разработано несколько способов защиты кузова от нее, причем встречаются как меры, направленные именно против данного явления, так и комплексные технологии защиты автомобиля, предохраняющие его от различных факторов. В приведенной статье рассмотрена электрохимическая защита кузова.
Причины образования коррозии
Так как электрохимический способ защиты автомобиля направлен исключительно против коррозии, следует рассмотреть причины, вызывающие поражение ею кузова. Основными из них являются вода и дорожные реагенты, применяемые в холодный период. В сочетании друг с другом они образуют высококонцентрированный соленый раствор. К тому же осевшая на кузове грязь продолжительное время удерживает влагу в порах, а если она содержит дорожные реагенты, то еще и притягивает молекулы воды и из воздуха.
Ситуация усугубляется, если лакокрасочное покрытие автомобиля имеет дефекты, даже небольшого размера. В таком случае распространение коррозии будет происходить очень быстро, и даже сохранившиеся защитные покрытия в виде грунта и оцинковки могут не остановить этот процесс. Поэтому важно не только постоянно очищать автомобиль от грязи, но и следить за состоянием его лакокрасочного покрытия. В распространении коррозии также играют роль температурные колебания, а также вибрации.
Также следует отметить участки автомобиля, наиболее подверженные поражению коррозией. К ним относятся:
- детали, расположенные ближе всего к дорожному покрытию, то есть пороги, крылья и днище;
- сварные швы, оставшиеся после ремонта, особенно если он был неграмотно осуществлен. Это объясняется высокотемпературным «ослаблением» металла;
- кроме того, ржавчина часто поражает различные скрытые плохо вентилируемые полости, где скапливается влага и долго не высыхает.
Принцип действия электрохимической защиты
Рассматриваемый способ защиты кузова от ржавчины относят к активным методам. Разница между ними и пассивными способами состоит в том, что первые создают какие-либо защитные меры, не позволяющие вызывающим коррозию факторам воздействовать на автомобиль, в то время как вторые лишь изолируют кузов от воздействия атмосферного воздуха. Данная технология изначально применялась для защиты от ржавчины трубопроводов и металлоконструкций. Электрохимический метод считают одним из наиболее эффективных.
Разница между ними и пассивными способами состоит в том, что первые создают какие-либо защитные меры, не позволяющие вызывающим коррозию факторам воздействовать на автомобиль, в то время как вторые лишь изолируют кузов от воздействия атмосферного воздуха. Данная технология изначально применялась для защиты от ржавчины трубопроводов и металлоконструкций. Электрохимический метод считают одним из наиболее эффективных.
Данный способ защиты кузова, который также называют катодным, основан на особенностях протекания окислительно-восстановительных реакций. Суть состоит в том, что на защищаемую поверхность накладывают отрицательный заряд.
Сдвиг потенциала осуществляют с применением внешнего источника постоянного тока или путем соединения с протекторным анодом, состоящим из более электроотрицательного металла, чем защищаемый объект.
Принцип действия электрохимической защиты автомобиля состоит в том, что между поверхностью кузова и поверхностью окружающих объектов вследствие разности потенциалов между ними по цепи, представленной влажным воздухом, проходит слабый ток.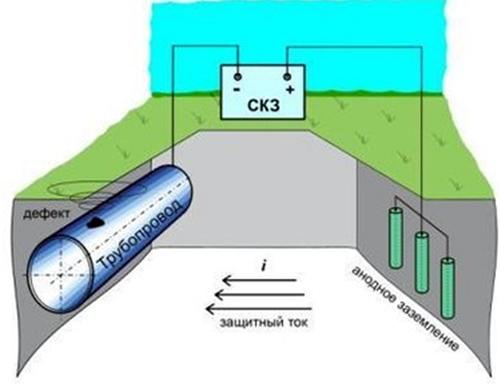 В таких условиях окислению подвергается более активный металл, а другой, наоборот, восстанавливается. Именно поэтому используемые для автомобилей защитные пластины из электроотрицательных металлов называют жертвенными анодами. Однако при чрезмерном сдвиге потенциала в отрицательную сторону возможно выделение водорода, изменение состава приэлектродного слоя и прочие явления, которые приводят к деградации защитного покрытия и возникновению стресс-коррозии защищаемого объекта.
В таких условиях окислению подвергается более активный металл, а другой, наоборот, восстанавливается. Именно поэтому используемые для автомобилей защитные пластины из электроотрицательных металлов называют жертвенными анодами. Однако при чрезмерном сдвиге потенциала в отрицательную сторону возможно выделение водорода, изменение состава приэлектродного слоя и прочие явления, которые приводят к деградации защитного покрытия и возникновению стресс-коррозии защищаемого объекта.
Рассматриваемая технология для автомобилей предполагает использование в качестве катода (отрицательно заряженного полюса) кузова, а анодами (положительно заряженными полюсами) служат различные окружающие объекты или установленные на автомобиле элементы, проводящие ток, например, металлические сооружения или влажное дорожное покрытие. При этом анод должен состоять из активного металла, такого как магний, цинк, хром, алюминий.
Во многих источниках приведена разность потенциалов между катодом и анодом. В соответствии с ними, чтобы создать полную защиту от коррозии для железа и его сплавов, необходимо достичь потенциал в 0,1-0,2 В. Большие значения слабо сказываются на степени защиты. При этом плотность защитного тока должна составлять от 10 до 30 мА/м².
В соответствии с ними, чтобы создать полную защиту от коррозии для железа и его сплавов, необходимо достичь потенциал в 0,1-0,2 В. Большие значения слабо сказываются на степени защиты. При этом плотность защитного тока должна составлять от 10 до 30 мА/м².
Однако эти данные не совсем верны – в соответствии с законами электрохимии, расстояние между катодом и анодом прямо пропорционально определяет величину разницы потенциалов. Поэтому в каждом конкретном случае необходимо достичь определенного значения разницы потенциалов. К тому же воздух, рассматриваемый при данном процессе в качестве электролита, способен проводить электрический ток, характеризующийся большой разницей потенциалов (примерно кВт), поэтому ток с плотностью 10-30 мА/м² не будет проводиться воздухом. Возможно возникновение лишь «побочного» тока в результате намокания анода.
Что касается разности потенциалов, наблюдается концентрационная поляризация по кислороду. При этом попавшие на поверхность электродов молекулы воды ориентируются на них таким образом, что происходит освобождение электронов, то есть реакция окисления. На катоде данная реакция, наоборот, прекращается. Вследствие отсутствия электрического тока освобождение электронов происходит медленно, поэтому процесс безопасен и незаметен. Благодаря эффекту поляризации, происходит дополнительное смещение потенциала кузова в отрицательную сторону, что дает возможность периодически выключать устройство защиты от коррозии. Нужно отметить, что площадь анода прямо пропорционально определяет эффективность электрохимической защиты.
На катоде данная реакция, наоборот, прекращается. Вследствие отсутствия электрического тока освобождение электронов происходит медленно, поэтому процесс безопасен и незаметен. Благодаря эффекту поляризации, происходит дополнительное смещение потенциала кузова в отрицательную сторону, что дает возможность периодически выключать устройство защиты от коррозии. Нужно отметить, что площадь анода прямо пропорционально определяет эффективность электрохимической защиты.
Варианты создания
В любом случае роль катода будет выполнять кузов автомобиля. Пользователю необходимо выбрать предмет, который будет использован в качестве анода. Выбор осуществляют на основе условий эксплуатации автомобиля:
- Для автомобилей, находящихся в неподвижном состоянии, на роль катода подойдет расположенный вблизи металлический объект, например, гараж (при условии, что он построен из металла или имеет металлические элементы), контур заземления, который может быть установлен в отсутствии гаража на открытой стоянке.

- На движущемся автомобиле могут быть использованы такие приспособления, как резиновый металлизированный заземляющийся «хвост», протекторы (защитные электроды), монтируемые на кузов.
Ввиду отсутствия тока, протекающего между электродами, бортовую сеть автомобиля +12 вольт достаточно подключить к одному или нескольким анодам через добавочный резистор. Последнее устройство служит для ограничения тока разряда аккумулятора в случае замыкания анода на катод. Основными причинами замыкания являются неграмотно осуществленная установка оборудования, повреждение анода или его химическое разложение вследствие окисления. Далее рассмотрены особенности применения перечисленных ранее предметов в качестве анодов.
Использование гаража в качестве анода считают наиболее простым способом электрохимической защиты кузова стоящего автомобиля. Если помещение имеет металлический пол или напольное покрытие с открытыми участками железной арматуры, то также будет обеспечена и защита днища. В теплый период в металлических гаражах наблюдается парниковый эффект, однако в случае создания электрохимической защиты он не разрушает автомобиль, а наоборот направлен на защиту его кузова от коррозии.
В теплый период в металлических гаражах наблюдается парниковый эффект, однако в случае создания электрохимической защиты он не разрушает автомобиль, а наоборот направлен на защиту его кузова от коррозии.
Создать электрохимическую защиту при наличии металлического гаража весьма просто. Для этого достаточно подключить данный объект к положительному разъему аккумуляторной батареи автомобиля через добавочный резистор и монтажный провод.
В качестве положительного разъема можно использовать даже прикуриватель при условии наличия в нем напряжения при отключенном замке зажигания (не у всех автомобилей данное приспособление сохраняет работоспособность при отключенном двигателе).
Контур заземления при создании электрохимической защиты используют в качестве анода по тому же принципу, что рассмотренный выше металлический гараж. Различие состоит в том, что гараж защищает весь кузов автомобиля, в то время как этот способ — лишь его днище. Контур заземления создают путем забивания в грунт по периметру автомобиля четырех металлических стержней длиной не менее 1 м и натягивания между ними проволоки. Подключение контура к автомобилю, как и гаража, осуществляют через добавочный резистор.
Контур заземления создают путем забивания в грунт по периметру автомобиля четырех металлических стержней длиной не менее 1 м и натягивания между ними проволоки. Подключение контура к автомобилю, как и гаража, осуществляют через добавочный резистор.
Резиновый металлизированный заземляющий «хвост» является простейшим способом электрохимической защиты движущегося автомобиля от коррозии. Данное приспособление представляет собой резиновую полоску с металлическими элементами. Принцип его функционирования состоит в том, что в условиях высокой влажности между кузовом автомобиля и дорожным покрытием возникает разность потенциалов. Причем чем выше влажность, тем больше эффективность электрохимической защиты, создаваемой рассматриваемым элементом. Заземляющий «хвост» устанавливают в задней части автомобиля таким образом, чтобы на него попадали брызги воды, вылетающие при движении по мокрому дорожному покрытию из под заднего колеса, так как это повышает эффективность электрохимической защиты.
Достоинство заземляющего хвоста состоит в том, что, помимо функции электрохимической защиты, он избавляет кузов автомобиля от статического напряжения. Это особо актуально для транспорта, перевозящего топливо, так как электростатическая искра, являющаяся результатом накопления статического заряда в процессе движения, опасна для транспортируемого им груза. Поэтому приспособления в виде металлических цепей, волочащихся по дорожному покрытию, встречаются, например, на бензовозах.
В любом случае необходимо изолировать заземляющий хвост от кузова автомобиля по постоянному току и наоборот «закоротить» по переменному. Это достигают путем использования RC-цепочки, которая представляет собой элементарный частотный фильтр.
Защита автомобиля от коррозии электрохимическим способом с использованием в качестве анодов защитных электродов рассчитана также на эксплуатацию в движении. Протекторы устанавливают в наиболее уязвимых для коррозии местах кузова, представленных порогами, крыльями, днищем.

Защитные электроды, как и во всех рассмотренных ранее случаях, функционируют по принципу создания разницы потенциалов. Достоинство рассматриваемого способа состоит в постоянном наличии анодов вне зависимости от того, стоит ли автомобиль или движется. Поэтому данную технологию считают весьма эффективной, однако она наиболее сложна в создании. Это объясняется тем, что для обеспечения высокой эффективности защиты необходимо установить на кузове автомобиля 15-20 протекторов.
В качестве защитных электродов могут быть использованы элементы из таких материалов, как алюминий, нержавеющая сталь, магнетит, платина, карбоксил, графит. Первые два варианта относят к разрушающимся, то есть состоящие из них защитные электроды требуется менять с интервалом в 4-5 лет, в то время как остальные называют неразрушающимися, так как они характеризуются значительно большей долговечностью. В любом случае протекторы представляют собой пластины круглой или прямоугольной формы площадью 4-10 см².
В процессе создания такой защиты нужно учитывать некоторые особенности протекторов:
- радиус защитного действия распространяется на 0,25-0,35 м;
- электроды необходимо устанавливать лишь на участки, имеющие лакокрасочное покрытие;
- для закрепления рассматриваемых элементов следует использовать эпоксидный клей или шпатлевку;
- перед установкой рекомендуется зачистить глянец;
- наружную сторону протекторов недопустимо покрывать краской, мастикой, клеем и прочими электроизоляционными веществами;
- так как защитные электроды представляют собой положительно заряженные пластины конденсатора, они должны быть изолированы от отрицательно заряженной поверхности кузова автомобиля.
Роль диэлектрической прокладки конденсатора будет выполнять лакокрасочное покрытие и клей, расположенные между протекторами и кузовом автомобиля. Также нужно учитывать, что величина расстояния между протекторами прямо пропорционально определяет электрическое поле, поэтому их следует устанавливать на небольшом расстоянии друг от друга, чтобы обеспечить достаточную емкость конденсатора.
Провода к защитным электродам подводят через проколы в закрывающих отверстия в днище автомобиля резиновых заглушках. Можно установить на автомобиль много протекторов маленького размера или меньшее количество защитных электродов большего размера. В любом случае необходимо использовать данные элементы на участках, наиболее уязвимых по отношению к коррозии, обращенными наружу, так как роль электролита в данном случае выполняет воздух.
Кузов автомобиля после установки электрохимической защиты такого типа не будет бить током, так как она создает электричество очень небольшой силы. Даже если человек прикоснется к защитному электроду, то не получит удар. Это объясняется тем, что в электрохимической антикоррозийной защите применяется постоянный ток малой силы, создающий слабое электрическое поле. К тому же существует альтернативная теория, согласно которой магнитное поле существует только между поверхностью кузова и местом установки защитных электродов. Поэтому электромагнитное поле, создаваемое электрохимической защитой, более чем в 100 раз слабее электромагнитного поля мобильного телефона.
Интересное по теме:
— «-» : ,
КаПроЗа-Лайт:
— Уменьшает скорость коррозии на 300-500%.
— Увеличивает ресурс кузова автомобиля в несколько раз.
Устройство электрохимической защиты автомобиля от коррозии «КаПроЗа-Лайт» предназначено для предохранения от дальнейшего распространения коррозии на деталях кузова автомобиля массой до 2 тонн. Действие устройства распространяется на большую часть поверхности кузова, в том числе недоступные и труднодоступные места, такие как днище автомобиля, внутренние части передних и задних крыльев, пороги, пол в салоне, внутренняя поверхность крышки багажника и капота, задние стенки багажного отделения, потолок салона, внутренние поверхности дверей, а также защищает от коррозии поврежденные в результате аварии части кузова.
В основу работы устройства «КаПроЗа-Лайт» положен принцип катодной поляризации металла кузова и создании гальванической пары между кузовом автомобиля и дополнительным электродом. Путем создания небольшого отрицательного потенциала (0,1-0,2 В) на кузове автомобиля процесс окисления металла практически прекращается. При катодной поляризации железу устройством сообщается такой отрицательный потенциал, при котором его окисление становится термодинамически маловероятным. Кроме того, за счет разрушения цинковых протекторов происходит замещение ионов железа ионами цинка (оцинковка).
Компплект «КаПроЗа-Лайт» состоит:
1) Из электронного блока формирования защитного потенциала, двух проводов (желтый и красный) с бензомаслостойкой изоляцией и гибкого спуска (трос в оплетке ПВХ) на анод, в качестве которого выступает земля;
2) Коррозийных протекторов (двух пластин массой 500 гр. каждая), закрепляемых по углам прямоугольника на днище автомобиля болтовым соединением. При этом место контакта днища должно быть зачищено до металлического блеска.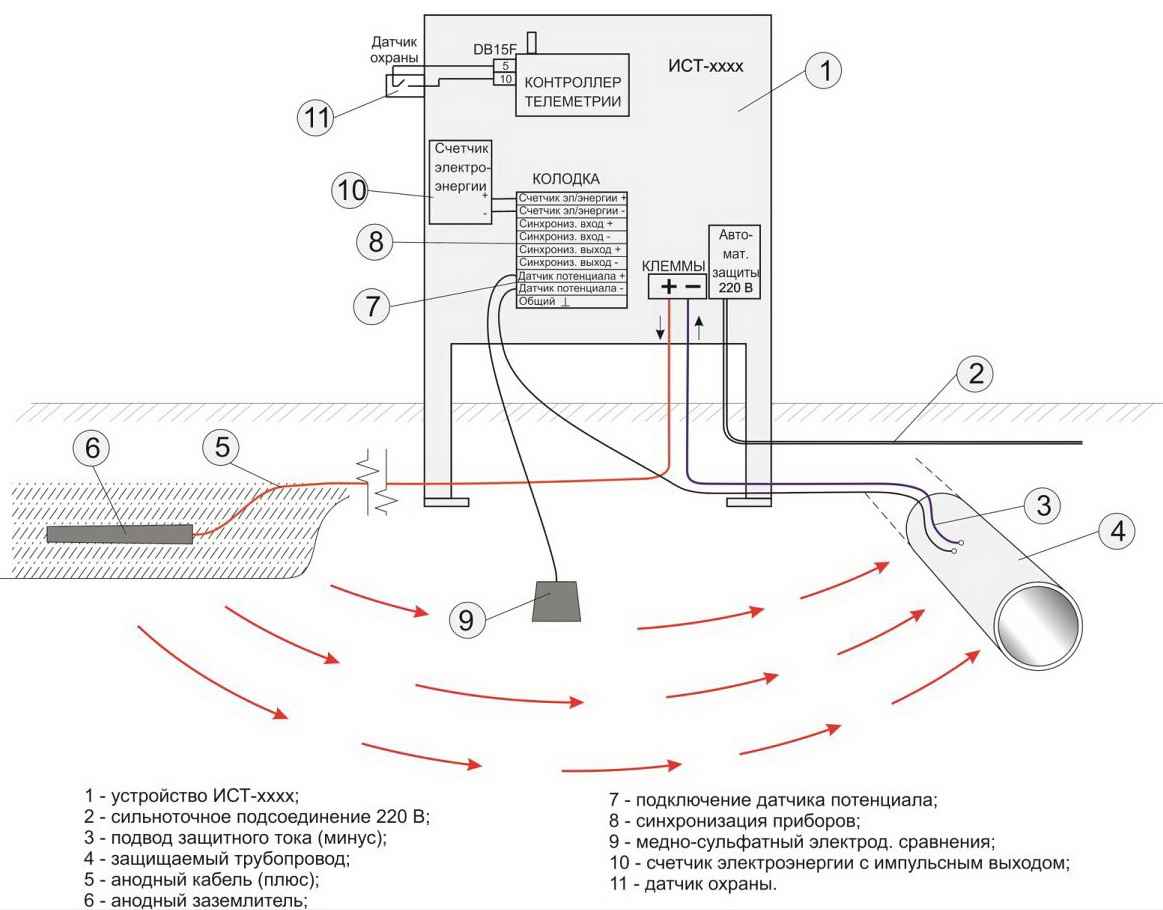 Гальваническая пара материалов днища и пластин создаёт ток, разрушающий пластины и защищающий кузов от коррозии. Один раз в два года необходимо очищать место контакта пластин и днища от грязи и выправлять напильником (или наждачной бумагой) образовавшиеся неровности на поверхности каждой пластины.
Гальваническая пара материалов днища и пластин создаёт ток, разрушающий пластины и защищающий кузов от коррозии. Один раз в два года необходимо очищать место контакта пластин и днища от грязи и выправлять напильником (или наждачной бумагой) образовавшиеся неровности на поверхности каждой пластины.
Подробная информация
Характеристики
| Страна производитель | Беларусь |
| Источник питания (электронный блок) | 12 В, DC, бортовая сеть автомобиля |
| Потребляемый ток (электронный блок) | 5 мА |
| Потребляемая мощность (электронный блок) | 0,006 Вт |
| Плотность защитного тока (электронный блок) | 50 мкА/ м² |
| Металл протектора | цинк (Zn) |
| Масса протектора |
500 гр.
|
| Токоотдача протектора | 820 А∙ч/кг |
| Стационарный потенциал Uн | -0,76 В |
| Плотность защитного тока (протектора) | 25 мА/м² |
| Защищаемая площадь поверхности | 7 м² (один протектор) |
| Срок службы (протектора) | 10 лет (ориентировочно) |
| Количество протекторов в комплекте | 2 шт. |
| Снижение скорости коррозии | 490,3 % (4,9 раза) |
Средства защиты коммуникаций от коррозии
Коррозия — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Скорость коррозии, как и всякой химической реакции, очень сильно зависит от температуры. Повышение температуры на 100 градусов может увеличить скорость коррозии на несколько порядков.
Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Скорость коррозии, как и всякой химической реакции, очень сильно зависит от температуры. Повышение температуры на 100 градусов может увеличить скорость коррозии на несколько порядков.
Справка. Антикоррозионная защита
«Мосинжпроект», не являясь профильным институтом, выступил с разработками в области защиты трубопроводов от коррозии и предоставил их в качестве основы для использования при проектировании объектов специалистам МосгазНИИпроекта и МосводоканалНИИпроекта.
Обеспечение антикоррозионной защиты – одно из важных направлений при проектировании, строительстве и эксплуатации объектов городской инженерной инфраструктуры. Актуальными эти вопросы становятся уже на этапе проектирования. Выверенные и обоснованные технические решения, заложенные в проект, гарантируют безопасность и долговременность эксплуатации объекта.
Актуальными эти вопросы становятся уже на этапе проектирования. Выверенные и обоснованные технические решения, заложенные в проект, гарантируют безопасность и долговременность эксплуатации объекта.
Этим направлением инженерии с момента основания «Мосинжпроекта» занимается мастерская №9, в составе которой выделено проектное и одновременно научно-экспериментальное подразделение. Именно «Мосинжпроект», не являясь профильным институтом, выступил с разработками в области защиты трубопроводов от коррозии и предоставил их в качестве основы для использования при проектировании объектов специалистам МосгазНИИпроекта и МосводоканалНИИпроекта.
Специалисты института применяют целый комплекс решений в области антикоррозийной защиты. Выбор конкретного решения зависит от многих факторов, таких как срок предполагаемой службы объекта, район, в котором размещается данный объект, особенности эксплуатации.
Современная защита металлов от коррозии осуществляется с помощью различных методов. Средства защиты можно разделить на две группы:
Средства защиты можно разделить на две группы:
— метод повышения химического сопротивления конструкционных материалов и изоляции поверхности металла от агрессивной среды, который обычно реализуется до начала производственной эксплуатации металлоизделия. Еще на стадии проектирования и изготовления изделия производится выбор конструкционных материалов и их сочетаний, наносятся гальванические и иные защитные покрытия;
— метод понижения агрессивности производственной среды и снижения коррозии наложением внешнего тока. Он осуществляется только в ходе эксплуатации металлоизделия и не связан с какой-либо предварительной обработкой до начала использования. Этот метод подразумевает пропускание тока через металл для достижения защитного потенциала, а также введение в технологическую среду специальных добавок-ингибиторов.
За 55 лет работы «Мосинжпроекта» мастерской выпущено более 4500 тысяч проектов по электрозащите подземных стальных коммуникаций от коррозии. В настоящий момент в Москве работает около 3000 водопроводных УКЗ и более 5000 установок защиты на газопроводных сетях, которые защищают порядка 45000 км стальных газопроводов, водопроводов, канализации и других металлических коммуникаций. За эти годы для Москвы сэкономлены сотни тонн металла.
За эти годы для Москвы сэкономлены сотни тонн металла.
Служба защиты от коррозии — АО «Газпром газораспределение Тамбов»
В АО «Газпром газораспределение Тамбов» защиту подземных трубопроводов от электрохимической коррозии осуществляют специализированные структурные подразделения (службы), которые включают в себя участки по эксплуатации и ремонту средств электрохимической защиты (далее – ЭХЗ), по ремонту и строительству средств ЭХЗ и по приборному обследованию газопроводов. Помимо этого служба ЭХЗ дополнительно выполняет функции электроизмерительной лаборатории по проведению измерений в электроустановках напряжением до 1000 В.
Основной задачей службы ЭХЗ является поддержание в исправном состоянии средств ЭХЗ путем планирования и проведения на них работ по техническому осмотру, текущему и капитальному ремонту. Проводимый специалистами службы ЭХЗ мониторинг состояния изоляционных покрытий газопроводов и проверка их на герметичность, позволяют оперативно выявлять и анализировать причины возникновения нарушений и коррозийных повреждений на газопроводах. Подразделения ЭХЗ имеются в каждом филиале АО «Газпром газораспределение Тамбов».
Подразделения ЭХЗ имеются в каждом филиале АО «Газпром газораспределение Тамбов».
Служба ЭХЗ имеет возможность на договорной основе оказывать ряд услуг для физических и юридических лиц, промышленных предприятий и организаций, к которым относятся:
- выдача технических условий на установку средств ЭХЗ;
- проведение периодических технических осмотров станций катодной защиты, протекторных установок с измерением разности потенциалов в контрольно-измерительных пунктах и на контактных устройствах;
- выполнение работ по текущему и капитальному ремонтам средств ЭХЗ;
- строительство новых, реконструкция и перенос существующих средств ЭХЗ;
- проверка эффективности работы станций катодной защиты и протекторных установок, исправности электроизолирующих соединений;
- поддержание средств ЭХЗ в работоспособном состоянии;
- ремонт электронных блоков управления станций катодной защиты любой сложности;
- согласование проектов ЭХЗ газопроводов;
- ведение технического надзора за строительством электрозащитных установок, приемка их в эксплуатацию;
- проведение мероприятий по обеспечению безопасной эксплуатации средств ЭХЗ;
- проведение измерений сопротивления растекания заземляющих устройств;
- измерение сопротивления изоляции кабельных линий;
- измерение сопротивления металлосвязи;
- измерение удельного сопротивления грунта;
- измерение тока однофазного короткого замыкания в сетях с глухозаземленной нейтралью.
Катодная защита наложенным током | Защита от коррозии
Системы катодной защиты с наложенным током имеют преимущество использования внешнего источника питания для управления током. Это позволяет защитить практически любую конструкцию, независимо от ее размера или текущих требований, используя аноды с длительным сроком службы и источники питания соответствующего размера.
Коррозия металлов — это естественный электрохимический процесс, который вызывает окисление и разрушение металла под воздействием окружающей среды (обычно называемое ржавчиной.) Катодная защита (CP) — это средство предотвращения коррозии путем подачи электрического тока от внешнего источника (анода) через окружающую среду к защищаемой металлической конструкции. Этот защитный ток изменяет окружающую среду вокруг металла, останавливая реакцию коррозии. При правильном проектировании и применении системы катодной защиты останавливают процесс коррозии. Катодная защита используется для предотвращения коррозии в широком диапазоне применений, когда защищаемая конструкция окружена средой, допускающей протекание тока.К сожалению, подверженный атмосферным воздействиям металл не может быть катодно защищен, потому что воздух не является проводником электрического тока, но большинство подводных и заглубленных применений подходят для катодной защиты, включая трубопроводы, корабли, доки, причалы, резервуары для хранения и ряд других конструкций.
Основные виды катодной защитыСуществует два основных типа систем CP: гальванические (или жертвенные) и системы с наведенным током. В гальванических анодных системах (также называемых жертвенными анодными системами) используется металл, который по своей природе более отрицательный, чем защищаемый металл, и, таким образом, когда два металла электрически соединены друг с другом, ток течет от металла, который является более электрически отрицательным, к металлу, который более электрически положительный.Этот ток приводит к быстрому расходу анода, поэтому для описания этих анодных систем часто используется общий термин «расходуемый анод». Типичные гальванические аноды включают магний, цинк и алюминий, поскольку каждый из них имеет более отрицательное электрическое сопротивление, чем углеродистая сталь или другие стали.
Анодные системы с наведенным током отличаются от гальванических (расходных) систем, поскольку они используют внешний источник постоянного тока для создания электрического тока. Использование внешнего источника питания позволяет системе с подаваемым током генерировать значительно более высокий выходной ток с меньшим количеством анодов с более длительным сроком службы, чем любая система с протекторным анодом.
- Аноды с увеличенным сроком службы. Поскольку выбор анодов не зависит от электрического потенциала самого анода, аноды с подаваемым током могут быть выбраны на основе других факторов, таких как стоимость материала анода, плотность тока и нормы потребления. На сегодняшний день наиболее эффективными анодами являются аноды из смешанных оксидов металлов со стабильными размерами (MMO). Эти аноды имеют исключительно долгий срок службы по сравнению с другими вариантами анодов.
- Системы высокого тока. Основная формула для цепи постоянного тока состоит в том, что V = I x R (закон Ома), где V — разность напряжений или движущая сила, I — ток системы, а R — сопротивление системы.Сопротивление системы в значительной степени определяется окружающей средой, и его нелегко изменить. Для гальванических анодов значение V фиксировано и меньше 1 В, поэтому количество тока, которое может генерироваться гальваническим анодом, также ограничено. В системах ICCP управляющее напряжение является функцией размера выпрямителя cp, и типичные напряжения могут находиться в диапазоне от 20 В до 100 В. Намного больше, чем у любой гальванической системы.
- Расширенный контроль системы. В системе с гальваническим анодом существует очень ограниченное количество способов управления выходом системы.В большинстве гальванических систем они устанавливаются и оставляются для работы без каких-либо элементов управления. В некоторых случаях они работают так, как задумано, а в других случаях они либо работают слишком быстро, вызывая преждевременный выход из строя, либо работают недостаточно для защиты конструкции. Но после установки у вас мало контроля над их работой. В системе с подаваемым током источник питания можно отрегулировать для изменения тока, подаваемого в анодную систему. Если разряжается слишком большой ток, выходной сигнал источника питания системы может быть уменьшен, или, наоборот, если подаваемый ток недостаточен, то выходная мощность системы может быть увеличена (по крайней мере, до предела используемого источника питания.)
- Простота контроля и управления. Блок питания с системой подаваемого тока обеспечивает простое средство контроля и управления производительностью системы. После установки и надлежащего ввода в эксплуатацию выпрямитель системы катодной защиты с наложенным током обеспечивает легко проверяемую точку контроля. Ежемесячные показания выходного напряжения и тока источника питания можно проверять, чтобы убедиться в соответствии с предыдущими показаниями. При проектировании гальванической анодной системы требуются специальные условия для испытаний, чтобы подтвердить работоспособность системы.
MATCOR — лидер в разработке, производстве и установке систем катодной защиты наложенным током, в том числе:
Свяжитесь с нами по ссылке ниже, чтобы узнать, подходит ли система катодной защиты наложенным током для вашего применения.
Связаться со специалистом по коррозииЧто такое катодная защита? Какие плюсы и минусы?
Катодная защита является основным оружием против коррозии, но имеет некоторые дорогостоящие недостатки при попытке защитить более крупные стальные активы.
Для возникновения коррозии должны присутствовать четыре элемента: принимающая площадка, из которой течет ток, место назначения, где ток не течет, среда, способная проводить ток (например, вода, бетон или почва), и металлический путь между хост и целевой сайт.
Электрохимическая коррозия металлов — это процесс, при котором ионы на поверхности металла переносятся на другое вещество (деполяризатор, менее активное вещество или металл). Такими деполяризаторами являются кислород, кислоты или катионы более пассивных металлов.
Для чего используется катодная защита?
Катодная защита часто используется для уменьшения коррозионных повреждений активных металлических поверхностей. Он используется во всем мире для защиты трубопроводов, водоочистных сооружений, надводных и подводных резервуаров для хранения, корпусов судов и лодок, морских производственных платформ, арматурных стержней в бетонных конструкциях и опорах и т. Д.
Катодная система часто используется для защиты стали от коррозии. Коррозия возникает, когда два разнородных металла погружаются в электролитическое вещество, такое как вода, почва или бетон. Этот тип металлического проводящего пути между двумя разнородными металлами обеспечивает путь, по которому свободные электроны перемещаются от более активного металла (анода) к менее активному металлу (катоду). Если свободные электроны с анода не достигают активных центров катода до поступления кислорода, ионы в активных центрах могут затем рекомбинировать с образованием гидроксида железа, т.е.е. ржавчина.
Трубопровод с катодной защитой
Как работает катодная защита?
По сути, катодная защита соединяет основной металл, подверженный риску (сталь), с жертвенным металлом, который подвергается коррозии вместо основного металла. Метод обеспечения катодной защиты стали сохраняет металл, обеспечивая высокоактивный металл, который может действовать как анод и обеспечивать свободные электроны. Вводя эти свободные электроны, активный металл жертвует своими ионами и предохраняет менее активную сталь от коррозии.
Виды катодной защиты.
Существует два основных типа катодной защиты:
- Гальваника
- Катодная защита наложенным током.
Гальванический
Гальваническая защита заключается в нанесении на сталь защитного цинкового покрытия для предотвращения коррозии. Цинк корродирует вместо герметизированной стали. Эти системы имеют ограниченный срок службы. Жертвенный анод, защищающий лежащий под ним металл, со временем будет разрушаться.До тех пор, пока жертвенный анод не перестанет обеспечивать защиту.
Катодная защита наложенным током
Системы катодной защиты с наложенным током состоят из анодов, подключенных к источнику питания, который обеспечивает постоянный источник электрического тока. В методе защиты с протекторным анодом для «жертвоприношения» ионов используется металл, более активный, чем основной металл. Эти «расходуемые аноды» (обычные сплавы, такие как магний, алюминий или цинк) имеют более сильный электрохимический потенциал.Этот метод часто может обеспечить гораздо более длительную защиту, чем жертвенный анод. Анод питается от неограниченного источника питания.
Недостатки катодной защиты.
Катодная защита использовалась в течение многих лет для защиты конструкций, которые подвергаются длительному воздействию агрессивных сред. Но сама установка катодной защиты может быть дорогостоящей. Конкретные детали того, как строятся конструкции, также могут добавить сложности. Итак, стоимость катодной защиты.Помимо этой стоимости, система также требует регулярного обслуживания, включая периодический визуальный осмотр. В случае катодной защиты наложенным током также существуют текущие расходы на электроэнергию. В частности, расходные аноды имеют ограниченное количество доступных в настоящее время, они подвержены быстрой коррозии. Это означает, что у них ограниченная продолжительность жизни.
Эта защита плохо работает на больших металлических поверхностях, не имеющих барьерного покрытия. Ключевым примером является днище больших сварных резервуаров.Причина в том, что даже для хорошо спроектированной катодной системы практически невозможно поддерживать надлежащее напряжение на длинном неизолированном металлическом участке. Это происходит из-за естественного падения напряжения при протекании тока, и ток обязательно будет течь, когда поверхность соприкасается с землей и не изолирована. Хотя катодная защита может отлично работать на трубопроводах с эпоксидным барьерным покрытием, она имеет серьезные ограничения для поверхностей без покрытия. Специалисты считают катодную защиту второстепенной по сравнению с барьерным покрытием.
Испытательные панели с покрытием EonCoat Weldable Coating при сварке. Без повреждения покрытия.
Лучшее решение.
EonCoat — лучшее решение, чем катодная защита. После того, как вы нанесете покрытие на актив, его практически не потребуется обслуживать, и теперь с нашим покрытием EonCoat Weldable Coating. Днища резервуаров теперь имеют еще одну возможность защиты от коррозии. Катодная защита работает, но имеет свои ограничения. Эти ограничения преодолеваются с EonCoat.
Катодная защита 101
Ричард Бакстер и Джим Бриттон
Как сталь разъедает в воде?
Чтобы понять катодную защиту, вы должны сначала понять, как вызывается коррозия.Для возникновения коррозии должны присутствовать три вещи:
1. Два разнородных металла
2. Электролит (вода с любым типом соли или растворенных в ней солей)
3. Металлический (проводящий) путь между разнородными металлами
Два разнородных металла могут быть совершенно разными сплавами, такими как сталь и алюминий, но более вероятно, что это будут микроскопические или макроскопические металлургические различия на поверхности цельного куска стали. В данном случае мы будем рассматривать свободно корродирующую сталь, которая неоднородна.
Если указанные выше условия существуют, в более активных центрах протекает следующая реакция: (два иона железа плюс четыре свободных электрона).
2Fe => 2Fe ++ + 4e —
Свободные электроны перемещаются по пути металла к менее активным центрам, где происходит следующая реакция: (газообразный кислород превращается в ион кислорода — путем объединения с четырьмя свободными электронами — который соединяется с водой с образованием гидроксильных ионов).
O 2 + 4e — + 2H 2 0 => 4 OH —
Рекомбинация этих ионов на активной поверхности приводит к следующей реакции, в результате которой образуется гидроксид железа, продукт коррозии железа: (железо соединяется с кислородом и водой с образованием гидроксида железа).
2Fe + O 2 + 2H 2 O => 2Fe (OH) 2
Эта реакция чаще описывается как «протекание тока через воду от анода (более активный участок) к катоду (менее активный участок)».’
Как катодная защита останавливает коррозию?
Катодная защита предотвращает коррозию за счет преобразования всех анодных (активных) участков на поверхности металла в катодные (пассивные) за счет подачи электрического тока (или свободных электронов) от альтернативного источника.
Обычно это гальванические аноды, которые более активны, чем сталь. Эту практику также называют жертвенной системой, поскольку гальванические аноды жертвуют собой, чтобы защитить конструкционную сталь или трубопровод от коррозии.
В случае алюминиевых анодов реакция на поверхности алюминия: (четыре иона алюминия плюс двенадцать свободных электронов)
4Al => 4AL +++ + 12 e —
и на стальной поверхности: (газообразный кислород превращается в ионы кислорода, которые соединяются с водой с образованием гидроксильных ионов).
3O 2 + 12e — + 6H 2 0 => 12OH —
Пока ток (свободные электроны) достигает катода (стали) быстрее, чем кислород, коррозия не происходит.
Рисунок 1: Система расходуемого анода в морской водеОсновные соображения при проектировании расходуемых анодных систем
Электрический ток анодного разряда регулируется законом Ома:
I = E / R
I = текущий ток в амперах
E = разница потенциалов между анодом и катодом в вольтах
R = полное сопротивление цепи в омах
Первоначально ток будет высоким, потому что разница потенциалов между анодом и катодом велика, но по мере того, как разность потенциалов уменьшается из-за эффекта протекания тока на катод, ток постепенно уменьшается из-за поляризации катода.Сопротивление цепи включает как водный путь, так и металлический путь, который включает любой кабель в цепи. Преобладающей величиной здесь является сопротивление анода морской воде.
Для большинства применений сопротивление металла настолько мало по сравнению с водонепроницаемостью, что им можно пренебречь (хотя это не относится к саням или длинным трубопроводам, защищенным с обоих концов). Как правило, длинные и тонкие аноды имеют меньшее сопротивление, чем короткие толстые аноды. Они будут разряжать больше тока, но не так долго.
Следовательно, разработчик катодной защиты должен подобрать аноды так, чтобы они имели правильную форму и площадь поверхности для разрядки достаточного тока для защиты конструкции и достаточный вес, чтобы прослужить желаемый срок службы при разрядке этого тока.
Как правило:
Длина анода определяет, какой ток может производить анод, и, следовательно, сколько квадратных футов стали можно защитить. Поперечное сечение (вес) определяет, как долго анод может выдерживать этот уровень защиты.
Системы катодной защиты с постоянным током (анодные системы ICCP)
Из-за высоких токов, присутствующих во многих системах с морской водой, нередко используются системы с подаваемым током, в которых используются аноды того типа (аноды ICCP), которые нелегко растворяются в ионах металлов. Это вызывает альтернативную реакцию: окисление растворенных хлорид-ионов.
2Cl — => Cl 2 + 2e —
Питание осуществляется от внешнего блока питания постоянного тока.
Рисунок 2: Система катодной защиты наложенным током в морской водеКак узнать, достаточно ли у нас катодной защиты?
Мы можем проверить наличие достаточного тока, измерив потенциал стали относительно стандартного электрода сравнения, обычно серебра / хлорида серебра (Ag / AgCl SW.), Но иногда и цинка (SW.).
Поток тока на любой металл сместит его нормальный потенциал в отрицательную сторону.История показала, что если сталь получает достаточно тока, чтобы сместить потенциал до (-) 0,800 В по сравнению с серебром / хлоридом серебра (Ag / AgCl), коррозия практически останавливается.
Из-за природы образующихся пленок минимальный (-0,800 В) потенциал редко бывает оптимальным, поэтому разработчики стараются достичь потенциала между (-) 0,950 В и (-) 1,000 В относительно Ag / AgCl sw.
Рисунок 3: Защищенные и незащищенные конструкции, подтвержденные потенциалом катодной защитыОбъяснение катодной защиты — Cathwell
Катодная защита — это метод предотвращения коррозии подводных и подземных металлических конструкций.
Что такое катодная защита?Катодная защита — один из самых эффективных методов предотвращения коррозии металлической поверхности.
Катодная защита обычно используется для защиты от коррозии многочисленных конструкций, таких как корабли, плавучие средства для плавания в открытом море, подводное оборудование, гавани, трубопроводы, резервуары; в основном все подводные или заглубленные металлические конструкции.
Основные принципы катодной защиты
Метод основан на преобразовании активных областей на металлической поверхности в пассивные, другими словами, превращении их в катод электрохимической ячейки. Узнайте больше об электрохимических элементах и коррозии.
Путем подачи тока потенциал металла снижается, коррозия прекращается и достигается катодная защита. Катодная защита может быть обеспечена одним из следующих способов:
- Протекторная катодная защита анода
- Катодная защита наложенным током, часто обозначаемая как ICCP
Жертвенная катодная защита анода
Самый простой метод применения катодной защиты — соединение защищаемого металла с другим, более легко корродирующим металлом, который действует как анод.Цинк, алюминий и магний — металлы, обычно используемые в качестве анодов.
Подробнее о гальванических сериях и благородстве металлов.
Принципы жертвенной катодной защитыСамый активный металл (он также является менее благородным) становится анодом для других и жертвует собой, разъедая (отдавая металл), чтобы защитить катод. Отсюда и термин жертвенный анод.
Поскольку управляющее напряжение расходуемых анодов низкое по сравнению с анодами с подаваемым током, расходуемые аноды должны быть хорошо распределены и расположены ближе к защищаемой области.
Что использовать; алюминиевые или цинковые аноды в среде соленой воды?
Из-за разницы потенциалов между анодной (менее благородной) и катодной областями (сталь) положительно заряженные ионы металла покидают поверхность анода, а электроны покидают поверхность на катоде. Для анодов из алюминиевого сплава реакция на поверхности анода следующая: 4Al → 4Al + + + + 12e — .
Катодная защита с постоянным током (ICCP)
СистемыICCP используют внешний источник электроэнергии, обеспечиваемый регулируемым источником постоянного тока, часто называемым панелью управления.Панель управления обеспечивает ток, необходимый для поляризации защищаемой поверхности.
Принципы ICCP — катодная защита наложенным токомЗащитный ток распределяется с помощью специально разработанных инертных анодов, обычно из проводящего материала, который нелегко растворяется в ионах металлов, но поддерживает альтернативные анодные реакции.
Система ICCP непрерывно контролирует уровень защиты и адаптируется к току, необходимому для остановки коррозии.
В хороших условиях морской воды окисление растворенных ионов хлора будет преобладающей анодной реакцией, в результате которой на поверхности анода образуется газообразный хлор: 2Cl — → Cl 2 + 2e — . В водах с низкой соленостью преобладающей анодной реакцией будет разложение воды: 2H 2 O → O 2 + 4H + + 4e — .
Одним из наиболее распространенных типов анодов ICCP для применения в морской воде является «MMO / Ti», который состоит из титановой подложки (Ti), покрытой катализатором из благородного металла или оксида металла (MMO).
Когда достигается катодная защита?
Ток катодной защиты, протекающий по любому металлу, смещает его нормальный потенциал в отрицательном направлении. Полная катодная защита стали достигается за счет потенциала на определенном уровне. Подробнее об уровне катодной защиты.
Последнее обновление: 09.12.2019
Четыре шага к защите электрического оборудования от коррозии
При выборе электротехнической продукции для суровых условий эксплуатации решающее значение имеет выбор правильных материалов, обеспечивающих адекватную коррозионную стойкость.При морских нефтегазовых операциях оборудование находится под постоянным воздействием морской воды и солевых брызг, которые обладают высокой коррозионной активностью из-за автокаталитического действия хлорида натрия и других растворенных хлоридов.
Коррозионные вещества, такие как сероводород и диоксид углерода, также встречаются в природе на месторождениях нефти и газа. Другие коррозионные вещества, влияющие на широкий спектр отраслей промышленности, включают хлор, бром, соляную кислоту и аммиак.
Не во всех отраслях промышленности есть одинаковые проблемы с коррозией, но все отрасли должны серьезно относиться к возможности коррозии и выбирать правильные материалы и продукты для своих конкретных операций и окружающей среды.Всемирная организация по коррозии оценивает ежегодные мировые издержки от коррозии в 2,2 триллиона долларов, что составляет более 3 процентов мирового ВВП. Любые деньги, которые можно сэкономить за счет предотвращения коррозии, включая стоимость простоев, оплату труда и новое оборудование для замены вышедших из строя деталей, напрямую повышают прибыльность.
Коррозия может принимать разные формы, и правильный выбор материалов и отделки является ключом к предотвращению каждого из них. Appleton, мировой лидер в производстве электротехнической продукции для промышленных зон, предлагает следующие четыре совета по защите электрооборудования от коррозии:
1.) Выбор материалов по их гальваническим свойствам. У разных металлов и сплавов разные электродные потенциалы. Когда два разных металла электрически соединяются в присутствии электролита, такого как морская вода, более активный металл становится анодным, теряя электроны и повышая степень окисления в процессе, известном как гальваническая коррозия. В гальванической серии металлы классифицируются от благородных до активных в зависимости от силы ионной связи на поверхности. Относительно более благородный металл, такой как нержавеющая сталь, будет лучше сопротивляться коррозии, чем более активный металл, такой как чугун.Гальваническую коррозию можно минимизировать, выбирая металлы близко друг к другу в гальванической серии. В качестве альтернативы, более активный металл можно использовать в качестве расходуемого анода, который притягивает коррозию, чтобы защитить более благородный металл от агрессивного воздействия.
2.) Использование защитных покрытий. Могут применяться различные виды отделки, помогающие изолировать металлические поверхности от окружающей агрессивной среды. Самый известный пример — обычная краска, наносимая на сталь для предотвращения ржавчины, но есть много других методов, включая обожженную эмаль, эпоксидное порошковое покрытие и покрытие из ПВХ.Для эффективной защиты покрытия должны быть нанесены должным образом и защищены от повреждений во время установки и использования. Цинковая поверхность на оцинкованной стали служит одновременно и защитным покрытием, и, в случае повреждения, расходным анодом, который будет корродировать, а не оголенную сталь.
3.) Использование пассивации. Некоторые металлы образуют на поверхности слой оксида металла толщиной в несколько молекул в процессе, известном как пассивация. Это происходит естественным путем, но процесс также можно улучшить с помощью химической пассивации или анодирования.В отличие от обычной ржавчины, пассивированный слой плотно связан с поверхностью, предотвращая дальнейшее проникновение кислорода или коррозионных химикатов. Наиболее известными примерами являются алюминий и нержавеющая сталь, которые образуют пассивированные слои оксида алюминия и оксида хрома соответственно. Если поверхность повреждена, пассивированный слой обычно быстро восстанавливается. Однако неблагоприятные условия могут помешать процессу. Например, точечная коррозия может происходить в алюминии, подвергающемся воздействию морской воды, когда ионы хлора препятствуют пассивации.Сварная нержавеющая сталь может подвергаться коррозии, когда содержание углерода достаточно высоко для образования карбидов хрома, истощая хром, доступный для пассивации в зоне сварного шва, и обеспечивая гальваническую реакцию между участками с различным содержанием хрома. Однако при правильном выборе для предполагаемого применения пассивированные материалы могут обеспечить отличную защиту даже в высококоррозионных средах.
4.) Выбор неметаллических компонентов. Производители все чаще предлагают неметаллические изделия, полностью непроницаемые для окружающей среды и веществ, которые могут вызывать коррозию металлов.Однако неметаллические материалы могут подвергаться воздействию определенных химикатов, в зависимости от состава используемых пластиков. Подавляющее большинство приложений никогда не будут подвергаться воздействию этих веществ. Продолжительное воздействие УФ-излучения также может привести к разрушению пластика, и пользователи, проживающие в местах с высоким УФ-излучением, должны учитывать это в спецификациях своих материалов.
Emerson Industrial Automation
www.Emerson.com
Предотвращение коррозии | Введение в химию
Цель обучения
- Обсудите общие профилактические меры, которые можно предпринять против коррозии металлической поверхности
Ключевые моменты
- Для возникновения коррозии необходимы три фактора: электролит, открытая металлическая поверхность и акцептор электронов.
- Коррозию можно предотвратить, сняв одно из этих условий.
- Покрытие металлической поверхности краской или эмалью создает барьер между металлом и влагой окружающей среды.
- Процесс покрытия металлической поверхности другим металлом, который с большей вероятностью окисляется, называется жертвенным покрытием.
Условия
- жертвенное покрытие Металлическое покрытие, которое подвержено окислению с большей вероятностью, чем металл, который оно защищает.
- цинкование Для покрытия металла тонким слоем электрохимическим способом; к гальванике.
- электролит: Вещество, которое в растворе или в расплавленном состоянии ионизирует и проводит электричество.
Анализ коррозии
Мы узнали, что для анодной и катодной стадий коррозии необходимы три вещи: электролит, открытая металлическая поверхность и акцептор электронов. Отсюда следует, что мы можем предотвратить коррозию, удалив одно из этих важных условий.Самое простое условие для удаления — это оголенная металлическая поверхность.
Создание физического барьера
Покрытие металлической поверхности краской или эмалью создает барьер между металлом и влагой в окружающей среде, тем самым устраняя возможность контакта кислорода и влаги с металлом.
Жертвенные покрытия
Процесс покрытия металлической поверхности другим металлом, который с большей вероятностью окисляется, называется жертвенным покрытием.Сталь из сплава железа, подверженная коррозии, обычно покрывается цинком, более активным металлом, в процессе, известном как цинкование. Коррозия жертвенного цинка приводит к его окислению; железо восстанавливается, что делает его катодным и препятствует его коррозии.
Оцинкованная поверхность Защита сплавов железа покрытием из более активного металла посредством процесса цинкования предотвращает коррозию сплавов.Контраст с предыдущим сценарием можно увидеть, когда железо или железный сплав покрывают менее активным металлом, например оловом.Пока оловянное покрытие остается неповрежденным, коррозия невозможна. Однако, если оловянное покрытие ухудшится, обнажая лежащий под ним металл, произойдет коррозия. Это связано с тем, что обнаженное железо подвергается окислению и становится анодным. Олово принимает электроны от окисленного железа, и соблюдаются три критерия коррозии.
Катодная защита
Еще один способ защиты от коррозии — создание постоянного отрицательного электрического заряда на металле. Этот метод называется катодной защитой.Катодная защита воспроизводит эффект жертвенного покрытия, но с более активным металлом. Источником отрицательного заряда обычно является внешний источник постоянного тока. Катодная защита используется, в частности, для защиты подземных топливных баков и трубопроводов.
Пассивация
Пассивация — это процесс, при котором на металлической поверхности образуется тонкая пленка продуктов коррозии, служащая барьером против окисления. На формирование пассивирующего слоя влияют pH окружающей среды, температура и химические условия.Статуя Свободы, например, покрыта сине-зеленой патиной, вызванной несколькими химическими реакциями, которая защищает металлическую медь под ней.
Анодирование
Анодирование — это еще одна обработка поверхности, защищающая от коррозии. Защищаемый металл покрывается специальным веществом, а электрохимические условия регулируются таким образом, чтобы в оксидной пленке металла появлялись однородные поры шириной несколько нанометров. Эти поры позволяют образовываться оксидной пленке, более толстой, чем пассивирующий слой.Полученный защитный слой очень твердый и очень эластичный.
Жертвенная защита анода
По тому же принципу, что и временное пленочное покрытие, расходуемый анод, сделанный из металла, более активного, чем металл, который вы хотите защитить, можно использовать для предотвращения коррозии металлических конструкций, погруженных в воду или заглубленных в землю. Жертвенный анод подвергнется коррозии раньше, чем металл, который он защищает. Однако, как только расходуемый анод подвергнется коррозии, его необходимо заменить; в противном случае металл, который она защищает, тоже начнет разъедать.
Катодная защита предотвращает коррозию Гальванический расходный анод, прикрепленный к корпусу корабля; Здесь протекторный анод показывает коррозию, а металл, к которому он прикреплен, — нет. Анод, кусок более электрохимически «активного» металла, прикреплен к уязвимой поверхности металла, где он подвергается воздействию электролита; потенциал уязвимой поверхности поляризован, чтобы быть более отрицательным, пока поверхность не будет иметь однородный потенциал. На этом этапе устраняется движущая сила реакции коррозии с защищаемой поверхностью.Гальванический анод продолжает корродировать, расходуя материал анода, пока в конечном итоге его не нужно будет заменить, но катодный материал защищен.Коррозия представляет реальную угрозу целостности личного имущества, а также мостов, дорог и другой общественной инфраструктуры. Понимание и реализация стратегий предотвращения коррозии уменьшит как экономический ущерб, так и ущерб, связанный с безопасностью, связанный с процессом.
Показать источникиBoundless проверяет и курирует высококачественный контент с открытой лицензией из Интернета.Этот конкретный ресурс использовал следующие источники:
Советы по защите электрических компонентов и машин от коррозии
От мерцающих огней до остановившегося оборудования — электроника, которая не работает должным образом, является большой проблемой. На рабочем месте вы полагаетесь на то, что ваше оборудование работает именно так, как задумано. Любая ситуация, в которой это не так, приводит к потере времени и денег для вашей прибыли. Итак, что вызывает эти типы сбоев и ошибок и как лучше всего на них реагировать?
Хотя на этот вопрос может быть несколько возможных ответов, вполне возможно, что проблема в коррозии.Если ваши провода и электрические компоненты подверглись коррозии, это может нанести ущерб вашей электрической системе и, безусловно, может снизить вашу производительность на день или даже дольше.
После того, как началась коррозия, мало что нужно сделать, кроме как заменить поврежденные электрические компоненты. Здесь нет особого выбора. Тем не менее, где вы можете принять меры и установить контроль над своими электрическими цепями, так это предотвращение коррозии в будущем. Коррозия не должна наносить вред вашей электронике, и есть простые способы ее избежать.Чтобы помочь вам в этом, давайте рассмотрим наши основные способы предотвращения коррозии ваших электронных компонентов и металлических поверхностей, а также то, почему это так важно в первую очередь.
Сколько стоит коррозия?Все мы знаем, что коррозия может нанести непоправимый ущерб электрическим компонентам. Но как это конкретно влияет на вас, ваших сотрудников и ваш бизнес?
Во-первых, полезно понять, что такое коррозия и что она делает с вашим оборудованием.Помимо основной коррозии, которая повреждает открытые металлические поверхности, существует два основных типа коррозии, о которых вам нужно беспокоиться при работе с электроникой вашей компании:
1. Гальваническая коррозия
Природные электролиты в любой жидкости проникают в электронные компоненты, создавая непреднамеренные электронные потоки, которые отрывают медь от проводов в вашей электронике. После того, как эта медь будет отключена, запланированное электрическое соединение не может произойти, что в конечном итоге приведет к отказу устройства.Другими словами, жидкость нарушила соединение между двумя электрическими точками, так что электричество больше не может течь между ними.
2. Дендитрическая коррозия
Этот тип коррозии начинается так же. Электролиты в жидкости нарушают существующий поток электричества, удаляя оксид меди, покрывающий следы проводов. Однако вместо того, чтобы останавливаться на достигнутом и просто прерывать существующее соединение, эта проблема идет еще дальше.Он формирует новое непреднамеренное электрическое соединение, приводящее к разного рода незапланированным действиям в вашем устройстве или оборудовании. Очевидно, этот вид коррозии более сложен.
Вот лишь некоторые из негативных последствий, которые коррозия может иметь для вашего бизнеса или производственного предприятия:
- Повреждение или потеря электроники: Как мы упоминали ранее, коррозия может полностью разрушить вашу электронику, вызывая ее ослабление, неправильную работу или полную остановку работы.Поскольку электроника стоит недешево, это часто может стать серьезным финансовым ударом.
- Повреждение или потеря металлических конструкций: Хотя значительная часть мер по предотвращению коррозии и борьбе с ней сосредоточена вокруг ее воздействия на электронику, важно помнить, что коррозия также может разрушать металлические поверхности и конструкции. Коррозия способна полностью покрыть эти поверхности, ослабить их и даже разрушить.
- Затраты на техническое обслуживание, ремонт и замену: Возвращение поврежденного оборудования в рабочее состояние обходится дорого, как и покупка нового оборудования для замены поврежденного оборудования.Если на вашем рабочем полу свирепствует коррозия и многие предметы необходимо заменить или отремонтировать, эти расходы очень быстро начнут накапливаться.
- Дополнительные косвенные потери: Коррозия открывает двери для всех видов рисков. Пожары могут возникать из-за нестабильной электроники, утечки могут возникать из-за негерметичных труб, и в результате могут пострадать рабочие, что приведет к потере денег из-за компенсации рабочим и оплачиваемого отпуска по травмам. Есть даже вероятность судебных исков, если будут замешаны травмы.Все эти последствия могут быть результатом неконтролируемой коррозии на вашем предприятии.
Если в прошлом вы неоднократно испытывали проблемы с коррозией, должно быть ясно, что эта проблема не просто случайное разовое событие. Вероятно, существует основная проблема, которую необходимо решить, иначе вы рискуете, что коррозия будет возвращаться снова и снова. Один из лучших способов применить этот тип электронной защиты от коррозии — это защитить окружающую среду на вашем предприятии.Вот несколько конкретных способов сделать это:
1. Ограничение влажности
Влажность — это количество воды в воздухе. Если влажность высокая, это означает, что в воздухе много воды, и наоборот. Поскольку мы знаем, что чрезмерная вода является причиной коррозии, логично предположить, что высокий уровень влажности приведет к увеличению количества коррозии.
По этой причине одним из лучших способов предотвращения коррозии является снижение уровня влажности в помещении.Скорее всего, это будет включать в себя инвестиции в качественное оборудование для контроля климата, что может показаться серьезными расходами. Однако эти вложения защитят ваше оборудование на долгие годы и избавят вас от необходимости ремонтировать или заменять металлические и электронные компоненты.
2. Контроль температуры
Оборудование для контроля микроклимата также является отличным способом гарантировать, что общие условия, в которых должно находиться ваше оборудование и электроника, не будут чрезмерно суровыми. Ни сильная жара, ни сильный холод не подходят для вашей электроники, и, хотя ни один из них не вызовет коррозию сам по себе, они могут усугубить уже существующие условия.
3. Улучшение воздушного потока
Горячий, задушенный и рециркулированный воздух — это еще и верный путь к катастрофе, когда дело касается коррозии. Электроника, которая хранится в замкнутом пространстве с низкой воздухопроницаемостью и без естественного воздушного потока, будет испытывать негативные побочные эффекты. В качестве примера в меньшем масштабе представьте, что могло бы случиться, если бы вы заперли свой телефон в машине в знойный летний день, когда солнце светит через окна. Из-за высокой температуры в сочетании с отсутствием движения воздуха у телефона, вероятно, возникнут серьезные последствия.
Снижение воздействия загрязняющих веществХотя проблемы состояния и климата, безусловно, могут усугубить основные проблемы с коррозией, они не являются их основной причиной. Горячая среда не идеальна для электроники, но сама по себе не вызывает коррозии. Основным фактором, вызывающим коррозию, являются посторонние элементы, такие как пыль, химические вещества и другие загрязнители.
Вот лишь некоторые из вероятных виновников, которые могут зацепиться за ваши компоненты и вызвать коррозию:
- Аммиак
- Кальций
- Хлориды
- Магний
- Калий
- Натрий
- Сульфат
К сожалению, для усердного работника, пытающегося защитить свою электронику, все эти элементы и химические вещества присутствуют практически в любой окружающей среде в мире, независимо от того, насколько тщательно вы заботитесь.Невозможно полностью избавиться от них.
Однако важно понимать, что, хотя все эти элементы могут повредить вашу электронику, это, скорее всего, не будет агрессивным или даже чрезвычайно проблематичным без добавления высокой влажности. При добавлении влаги эти химические вещества станут гораздо более разрушительными и начнут разъедать вашу электронику.
Хотя полностью исключить эти химические вещества из окружающей среды невозможно, вы все же можете принять разумные меры для их минимизации.Вот лишь несколько вещей, которые вы можете сделать:
1. Регулярно очищайте оборудование
Нет необходимости оставлять грязь, ржавчину или остатки на вашем оборудовании. Работая аккуратно и осторожно, регулярно тщательно очищайте электронику. Удалите весь скопившийся на них материал и часто повторяйте эту очистку.
2. Держите свое оборудование подальше от любых очевидных загрязнений
Есть ли где-нибудь на вашем предприятии открытый поток жидкости? Какие-нибудь незакрепленные материалы, которые могут взлететь и прикрепиться к ближайшим объектам? Простая мера предосторожности — держать электронику подальше от этих сред.Хотя это не гарантирует, что ваша электроника безопасна, это снижает вероятность неосторожного контакта с нежелательными химическими веществами.
3. Удаление пятен после контакта
Иногда случаются аварии. Если произойдет какой-либо инцидент, когда на ваше оборудование пролилась жидкость или оно случайно вступит в контакт с каким-либо материалом, которого не должно быть, произведите уборку как можно скорее. Протрите электронное оборудование, удаляя все возможные остатки.Вы можете повторить это на следующий день, чтобы вдвойне убедиться, что вы удалили все следы оставшегося постороннего материала.
Рассмотрите возможность добавления дополнительной защитыХотя невозможно полностью устранить элементы, которые могут попытаться повредить вашу электронику, есть еще один шаг, который вы можете предпринять, и это добавить дополнительный уровень защиты и безопасности к вашему оборудованию. Чтобы наилучшим образом предотвратить коррозию на вашем предприятии, подумайте о приобретении некоторых из следующих профилактических мер:
1.Нажимаемые токи
Это неожиданное средство электронного контроля коррозии, но оно доказало свою эффективность во многих сценариях. Это влечет за собой генерацию нового электрического тока, равного по величине и силе существующему току, но текущего в противоположном направлении. Это очень деликатное решение, и к нему следует обращаться только тем, кто обладает обширными знаниями в области электротехники, поскольку неправильная реализация этого решения может фактически привести к повышенному уровню коррозии.
2. Жертвенные металлы
Если вы поместите сталь в контакт с другим металлом, вторичный металл защитит сталь от ржавчины и коррозии. Сама по себе сталь почти всегда подвергается коррозии, но присутствие другого металла защищает сталь. Вместо того чтобы поражать сталь, коррозия поражает другой металл. Вы можете обуздать эту тенденцию и использовать ее в своих интересах, облицовав стальные поверхности другими материалами, такими как цинк или магний.
Вы часто можете увидеть этот принцип в игре на корпусах кораблей.Эти корпуса могут казаться ржавыми снаружи, но в большинстве случаев корродирует только цинковый или магниевый корпус. Сталь под ним остается безопасной. Кроме того, некоторые инженеры используют эту идею, окрашивая стальные поверхности слоем на основе цинка, который защищает сталь.
3. Грунтовки
Праймеры— отличный способ защитить любую поверхность от коррозии, которая в противном случае может ослабить и повредить ее. Грунтовка создает буферный слой между поверхностью и всем остальным, что будет поверх нее.В данном случае это «все остальное» — это коррозия.
Primer действует как барьер между металлическими поверхностями и коррозией. Вместо того, чтобы накапливаться непосредственно на металле, коррозия не может пройти сквозь грунтовку, и, таким образом, ваши поверхности будут защищены. Праймер выполняет эту конкретную работу тремя разными способами:
- Грунтовочное покрытие помогает снизить скорость захвата кислорода и влаги из окружающей среды на металлической поверхности. Большая часть влаги из воздуха поглощается грунтовкой, предотвращая ее контакт с металлом.Это не останавливает коррозию, но замедляет ее.
- Покрытие также помогает замедлить скорость, с которой коррозионные элементы диффундируют через грунтовку и сталкиваются с металлической поверхностью. Опять же, это не устраняет коррозию, но помогает замедлить ее.
- Многие высококачественные грунтовки, созданные специально для этой цели, также обладают антикоррозийными свойствами, которые фактически изменяют свойства защищаемого металла. Другими словами, само покрытие может вызвать у металла высокий уровень электрического сопротивления, что делает его менее подверженным коррозии.
Доступно множество различных типов грунтовок и покрытий, и вам нужно будет выбрать для себя то, что лучше всего подходит для ваших нужд. При принятии этого решения следует помнить о следующих вещах:
- Эстетика: Насколько для вас важно, как выглядит финальное покрытие? Некоторые грунтовки более эстетичны, чем другие.
- Цена: Как выглядит ваш бюджет? У нас есть праймеры для всех по разным ценам.
- Экологические проблемы: Узнайте, что разрешено в вашем регионе, в соответствии с местными и государственными правилами. Вы можете обнаружить, что некоторые покрытия запрещены или могут применяться только с соблюдением определенных дополнительных мер предосторожности.
- Тип: Защитные грунтовки — это не универсальное решение. Существует много разных типов, и все они имеют несколько разные подходы к решению проблемы коррозии. Например, порошковые краски и хроматные конверсионные покрытия — это всего лишь два стиля, из которых вы можете выбрать.
Хотя коррозия может показаться просто уродливым пятном, которое ползет по вашим металлическим поверхностям или электронике, это гораздо больше. Он способен ослабить или разрушить конструкции и повредить электронику настолько сильно, что они станут непригодными для использования. Если вы позволите коррозии беспрепятственно распространиться по всему оборудованию, невозможно сказать, какой ущерб она может причинить.


 д.).
д.).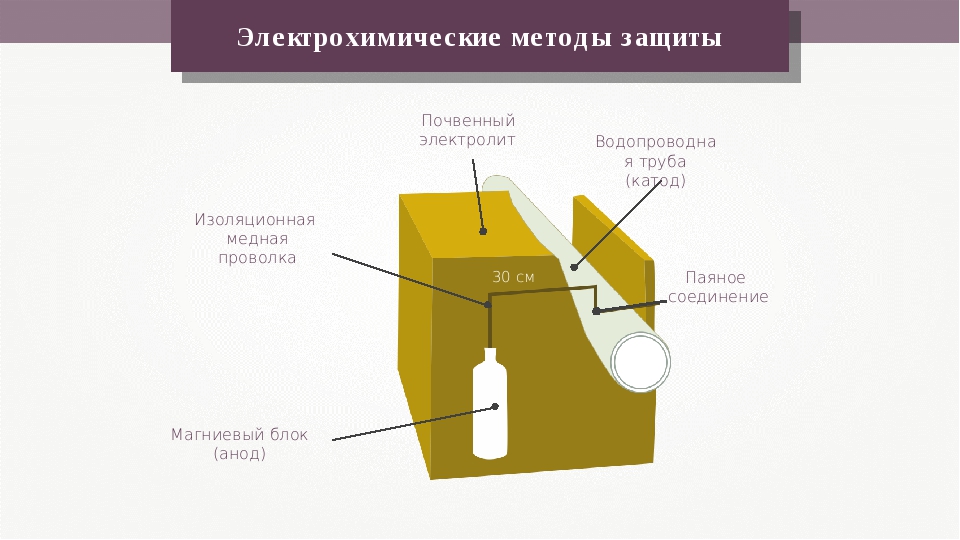
 В случае поляризованного дренажа ток течет только в одном направлении — от трубопровода к рельсу. Это не позволяет блуждающим токам натекать на трубопровод по дренажному проводу.
В случае поляризованного дренажа ток течет только в одном направлении — от трубопровода к рельсу. Это не позволяет блуждающим токам натекать на трубопровод по дренажному проводу. 
